- 关于我们
- 一站式服务
- 技术平台
临床研究
临床中心实验室
临床样本病理学检测
蛋白水平检测分析
免疫学细胞表现分型分析
药物毒性检测-CRS
TMB / 免疫微环境检测
血液疾病分型检测,类型鉴定
MRD(Minimal Residual Disease)
CART/TCRT/ADC/mAb/BisAb/
临床前研究
肿瘤疾病研究平台
小分子耐药模型
原位及转移模型
肿瘤模型 | 人源化小鼠
炎症&自身免疫疾病研究平台
脓毒症、多发性硬化症模型
炎症性肠病模型
系统性红斑狼疮、肾病模型
腹泻模型精神与神经系统:疾病研究平台
阿尔茨海默症、帕金森庄模型
疼瘾、抑郁证模型
精神分裂症、脑卒中、高血压模型
代谢疾病研究平台
肝纤维化、酒精性肝炎模型
非酒精性脂肪性肝炎(NASH)模型
急性肝损伤、肥胖模型
关节和骨疾病研究平台
关节炎、痛风,性关节炎、骨质疏松症模型
类冈湿关节炎模型
呼吸系统疾病研究平台
慢性组塞性肺病(COPD)模型
急性肺损伤模型
哮喘、肺纤维化模型
肺炎链球菌、肺支原体感染模型
肺铜绿盛染、肺曲霉感染模型
心血管系统疾病研究平台
高血压、高血脂模型
衰老、动脉粥样通化、缺血性脑损伤模型
皮肤系统疾病研究平台
银屑病、系统性硬化症模型
雄秃、斑秃模型
特应性皮炎、痤疮模型
医疗器械评价研究平台
全身毒性试验/急性、亚急性、亚慢性和慢性毒性试验
生物相容性评估
医美产品医疗器械有效性,安全性评估
药代动力学、安评
体内DMPK研究、体内DMPK研究
急毒,长毒,一般毒理
安全毒理、免疫原性评价
免疫毒性评价、非GLP毒理
- 加入我们
- 联系我们
news

(AD)特应性皮炎的新兴靶点和临床前OVA、DNFB、MC903动物模型验证策略
01 前言
皮肤瘙痒、红斑、反复发作,特应性皮炎患者们的噩梦即将结束?
特应性皮炎(Atopic dermatitis, AD)是一种常见的慢性、复发性、炎症性皮肤疾病,以剧烈瘙痒和湿疹样损害为主要特征。公开数据显示,我国当前特应性皮炎患者已超7000万,预计到2030年将达8170万人。特应性皮炎的治疗药物主要包括外用糖皮质激素、外用钙调磷酸酶抑制剂、口服抗组胺药、系统性免疫抑制剂等。然而,局部和全身应用糖皮质激素、免疫抑制剂等不良反应较多,且不宜长期使用。因此,开发局部给药且安全性更好的特应性皮炎治疗药物具有重要的临床意义。近年来,随着对AD发病机制理解的深化,众多新兴靶点如雨后春笋般涌现。除了传统的Th2型炎症通路,研究人员正在探索更多元的信号通路和治疗策略,为改善现有疗法不足的患者带来新希望。
02 AD药物研发新浪潮
从“广谱抗炎”到“精准打击”
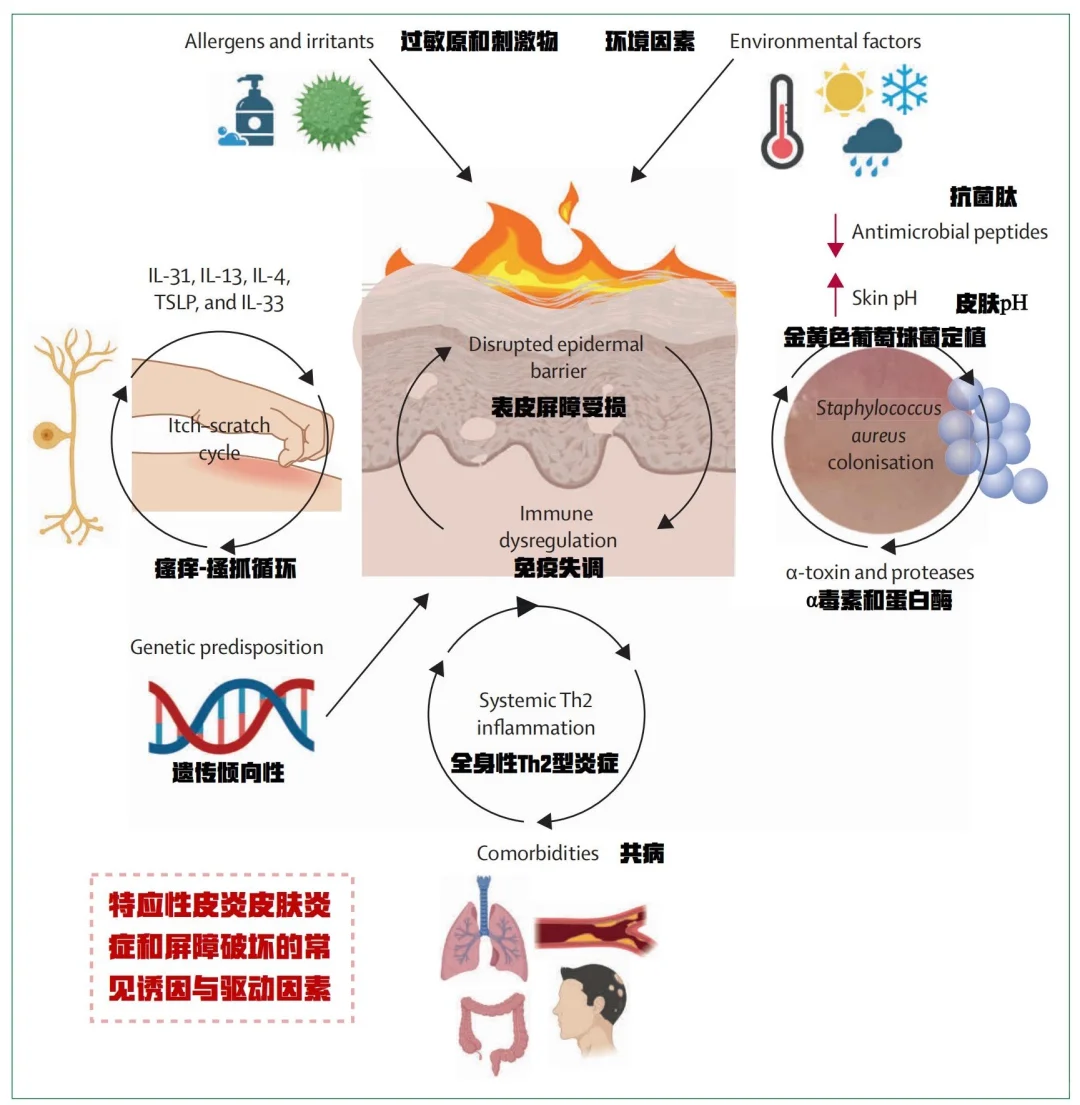
AD的发病机制可以概括为“皮肤屏障缺陷、免疫失调、微生物组失衡与神经信号异常”的恶性循环。过去几年,以度普利尤单抗(靶向IL-4Rα)和JAK抑制剂为代表的靶向药物取得了巨大成功,证明了精准治疗的可行性[1]。
然而,患者群体的异质性和未被满足的临床需求(如难治性瘙痒、特定内型患者疗效不佳等)驱动着研发人员探索更前沿的靶点。
03 引领未来的新靶点矩阵
我们将新兴靶点分为四大战略方向,为您勾勒出未来的研发蓝图:
1.根源修复:上皮屏障靶点
这类靶点旨在从根源上修复AD的皮肤屏障缺陷。
丝聚蛋白替代/功能增强:丝聚蛋白突变是AD最强的遗传风险因素,开发小分子伴侣蛋白能帮助突变丝聚蛋白正确折叠并发挥功能,或利用反义寡核苷酸技术,读取通义突变,产生全长功能性丝聚蛋白,挽救突变丝聚蛋白的功能。紧密连接调节蛋白:靶向Claudin-1等紧密连接蛋白,加固表皮细胞的第二道防线,减少外界过敏原的渗透。梁云生教授团队研究发现[2],度普利尤单抗可通过上调髓系树突状细胞(DCs)上的TIM-3,形成TGF-β1-TIM-3正反馈环,最终诱导DCs凋亡并抑制FcεRI表达,从而缓解炎症。研究团队通过分析AD患者在度普利尤单抗治疗前后的单细胞测序数据,结合空间转录组数据,发现度普利尤单抗显著上调髓系DCs上TIM-3的表达。此外,体内外实验揭示,Galectin-9和TGF-β1可以激活TIM-3通路,抑制FcεRI的表达和诱导髓系DCs凋亡,从而抑制AD炎症反应,这表明TGF-β1和Galectin-9可以作为AD治疗新靶点。
激肽释放酶抑制:抑制过度活跃的KLK5/KLK7等蛋白酶,防止它们降解角质层的关键成分(如角蛋白),从而稳定皮肤屏障。史玉玲教授团队与加州大学尔湾分校合作发现[3],OVOL1基因是表皮角质形成细胞中芳香烃受体(AhR)的一个关键直接靶点。研究表明,Ovol1的缺失不仅会削弱AhR在维持皮肤屏障功能中的作用,还会导致其下游靶点Id1的表达上调,从而加重AD皮肤炎症。进一步研究发现,ID1小分子抑制剂AGX51能显著改善小鼠AD样皮肤炎症。在人活检标本研究中,AGX51能调控细胞周期及炎症相关基因的表达。这些发现为AD治疗提供了潜在的新的靶点。
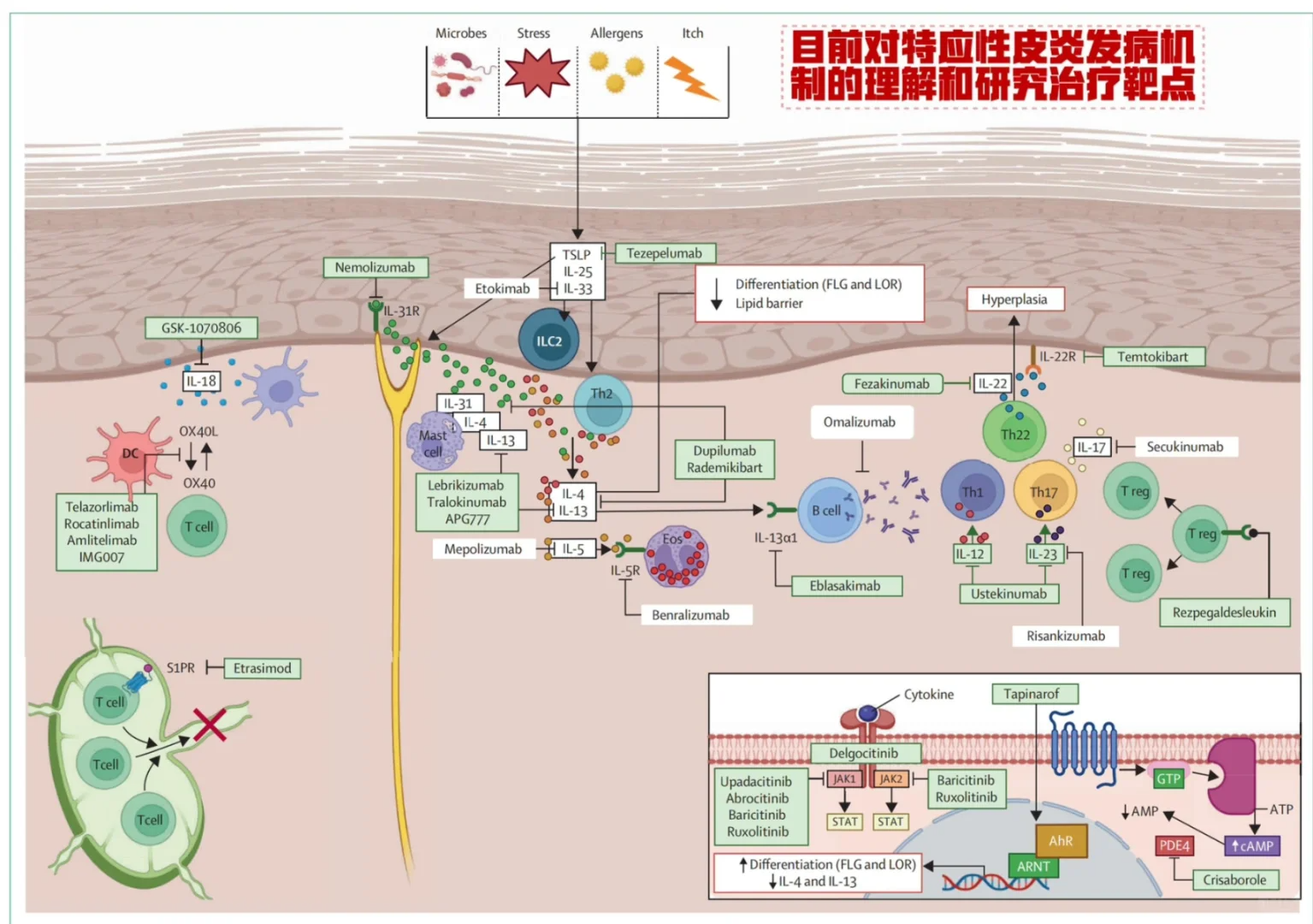
2. 免疫调控:超越2型免疫通路外的细胞因子靶点
在Th2轴之外,更多细胞因子被发现在AD,尤其是慢性、非典型或重症患者中扮演重要角色。
IL-13特异性亚型(IL-13δ): 这是一种天然的IL-13变异体,可能具有独特的病理作用,针对它的抗体可能提供更精准的阻断。再鼎医药研发的ZL-1503是一种创新的IL-13/IL-31R双特异性抗体,它能同步抑制AD的炎症通路和致痒通路[4]。现有IL-4/IL-13信号通路抑制剂虽然已显著改善AD治疗格局,但对由IL-31介导的某些AD症状只能部分缓解,导致现有疗法对许多患者起效慢且临床疗效有限。临床前研究表明,单次静脉注射ZL-1503可在非人灵长类动物中完全抑制IL-13介导的pSTAT6活化和IL-31诱导的抓挠行为至少76天,部分动物甚至持续超过118天和133天[5]。
TSLP/IL-33:作为启动2型免疫反应的上游关键分子,是拦截早期炎症的关键。
IL-22:由Th22细胞产生,直接参与角质形成细胞的异常增殖和分化,与表皮增生和苔藓化密切相关,是干预慢性AD的潜力靶点。
IL-31:直接作用于感觉神经元,是诱发瘙痒的关键细胞因子,阻断IL-31能有效缓解瘙痒,从而减少搔抓带来的皮肤屏障损伤。抗IL-31受体单抗(Nemolizumab)是Galderma公司研发的一款IL-31受体拮抗剂,通过阻断IL-31信号通路,显著减轻患者的瘙痒症状,并改善皮肤炎症。药物于2024年8月获FDA批准上市。
3. 直击症结:神经免疫与瘙痒靶点
旨在直接中断瘙痒信号,提高患者生活质量。
JAK1特异性抑制剂:JAK1作为IL-4、IL-13、IL-31、TSLP等多种瘙痒相关细胞因子信号的通路枢纽,JAK1抑制剂能从上游广谱抑制瘙痒。
PAR2/MrgprX2小分子拮抗剂或抗体:特异性瘙痒受体,可实现精准止痒且可能避免中枢副作用。
OX40受体靶向疗法:T细胞再平衡策略:靶向OX40受体的新型单抗Rocatinlimab(AMG 451/KHK4083)在中重度AD治疗中展现出突破性进展[6]。通过抑制致病性T细胞(包括Th1/Th2/Th17/Th22亚群)和减少记忆T细胞形成,该药物展现出独特的“T细胞再平衡”机制。IIb期试验数据显示,治疗16周时EASI评分改善达48.3%-61.1%(vs 安慰剂15.0%,P<0.001),瘙痒NRS评分降低25.6%-48.0%,且疗效持续至36周治疗期及20周停药后。这款非岩藻糖基化IgG1单抗通过直接阻断OX40-OX40L相互作用,减少致病T细胞活化,并降低血清Th2标志物和Th17标志物。
4. 微生态调节:精准抗菌
特异性清除或抑制AD皮损中过度增殖的金黄色葡萄球菌,而非广谱杀菌。
开发抗菌肽模拟物:设计类似人体天然抗菌肽的稳定分子。
靶向性溶菌酶等“生物导弹”:特异性裂解金黄色葡萄球菌的噬菌体溶菌酶。
04 派思维新的临床前验证策略
新兴靶点的验证需要一个多层次的、逐步深入的临床前研究体系。
1. 靶点发现与生物学确认
利用人类AD组学数据库分析,在原代角质形成细胞、神经元共培养体系等模型中,通过基因编辑、激动/拮抗实验,明确靶点的病理功能。
2. 体外药效学评估
在高通量筛选平台上,测试候选分子(如抗体、小分子)与其靶点的结合能力、亲和力和功能性抑制/激活效果。
3. 体内药效学与概念验证
这是临床前研究的核心,依赖于动物模型。自从将 Nc/Nga 小鼠描述为自发发生的 AD 模型以来,已经开发了许多 AD 小鼠模型。它们可分为三组:
- 表皮应用致敏剂诱导的模型
卵清蛋白(OVA)致敏/激发模型:通过卵清蛋白致敏和皮肤激发,模拟抗原驱动的AD。
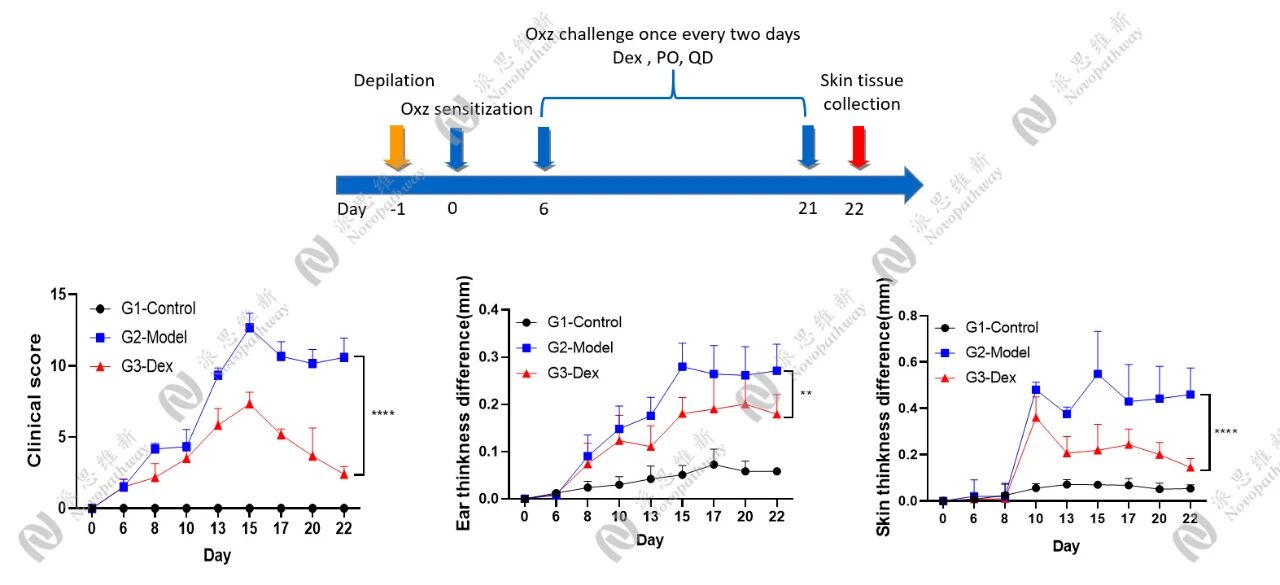
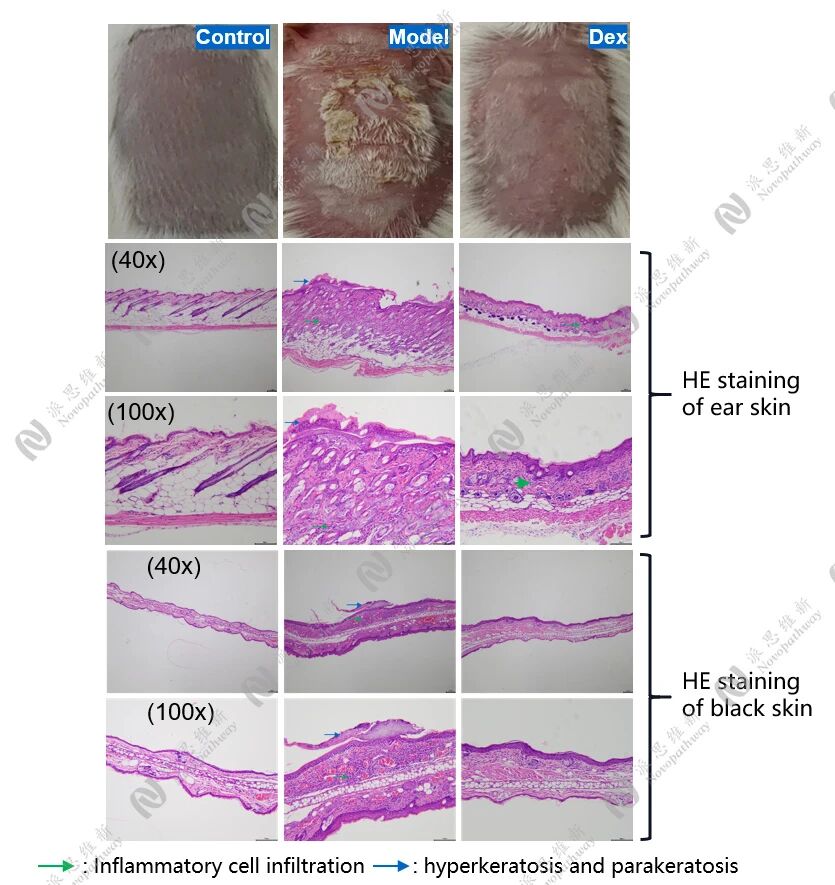
DNFB/oxazolone(2,4-二硝基氯苯/恶唑酮)模型:使用化学试剂反复刺激,这些小分子化学物质能与皮肤组织蛋白结合成为完全抗原,激活T淋巴细胞,引发过敏反应,诱导慢性皮炎。
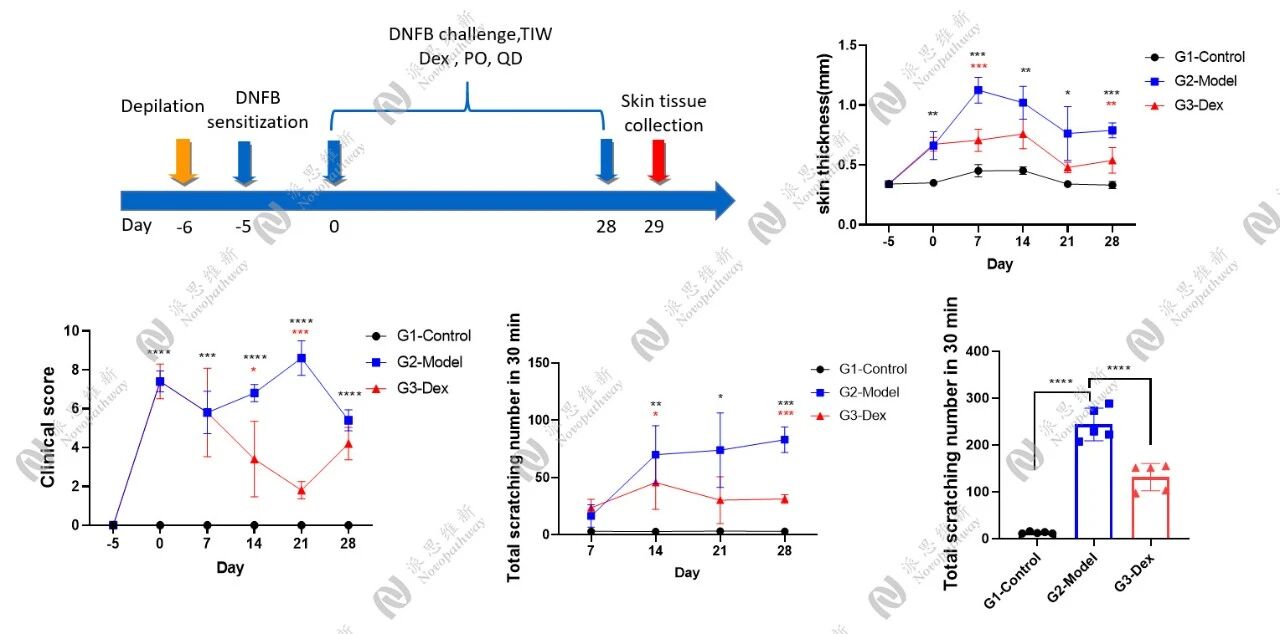
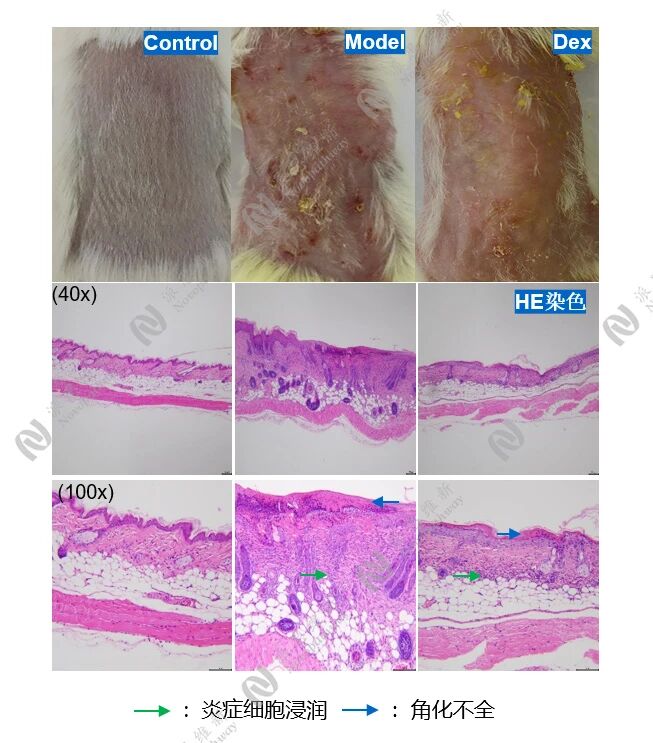
临床评分:评估红斑、水肿、表皮脱落、苔藓化的严重程度。瘙痒行为学: 记录搔抓次数。
分子生物学分析:取皮肤组织进行qPCR、ELISA、Western Blot,分析细胞因子水平、屏障蛋白表达。
组织病理学:H&E染色观察表皮增厚、炎症细胞浸润;免疫组化/免疫荧光观察特定蛋白的定位和表达。
皮肤屏障功能检测(TEWL测量):测量经皮水分流失率。
- 过度表达或缺乏选择性分子的转基因小鼠
Flaky Tail小鼠:天然携带丝聚蛋白突变,自发出现皮肤屏障缺陷和轻度炎症,评价药物对屏障的修复能力。
K14-IL-4/-IL-31转基因小鼠:在表皮特异性过表达IL-4或IL-31,分别模拟AD的炎症和瘙痒特征。
条件性基因敲除小鼠:例如,在皮肤中特异性敲除特定基因以研究其功能。
- 自发发生 AD 样皮肤病变的小鼠
4. 安全性评估:
(1)体外毒性筛选: 检测对肝细胞、心肌细胞等的细胞毒性。
(2)药理安全性: 评估候选药物对靶点在其他器官系统中可能产生的“脱靶”效应(例如,免疫抑制药物对宿主防御功能的影响)。
(3)动物毒理学研究: 在啮齿类和非啮齿类动物中进行短期和长期的毒理实验,确定最大耐受剂量和无观察不良反应水平。
05 未来与挑战
随着对AD发病机制认识的加深,新兴靶点药物研发呈现出多元化趋势。从传统的Th2炎症轴扩展到神经-免疫-皮肤屏障多重作用机制,为个体化治疗提供了可能。目前面临的挑战包括:如何精准识别最适合的患者人群;如何将临床前研究结果有效转化为临床疗效;以及如何评估长期安全性和疾病修饰潜力。随着这些新兴靶点药物逐步进入临床,预计未来5-10年AD治疗格局将发生显著变化,为患者提供更多有效、安全的治疗选择。
参考文献
[1]Langan, S. M,et al. Atopic dermatitis. The Lancet,2020,396 (10247) ,345-360.
[2]Yishan Chen, et al. Dupilumab-induced inhibition of myeloid dendritic cell function via TIM-3-TGF-β1 feedback loop in treatment of atopic dermatitis,J Allergy Clin Immunol, 2025 Sep;156(3),719-733.
[3]Zeyu Chen,et al.The AhR-Ovol1-Id1 regulatory axis in keratinocytes promotes epidermal and immune homeostasis in atopic dermatitis-like skin inflammation.Cell Mol Immunol,2025 Mar;22(3),300-315.
[4]再鼎医药在2025欧洲过敏与临床免疫学会(EAACI)大会上公布IL-13/IL-31R双抗ZL-1503治疗特应性皮炎的临床前新数据。(2025-06-13)
[5]Bieber, T. Interleukin-13: Targeting an underestimated cytokine in atopic dermatitis.Allergy, 2022, 77 (6), 1725-1739.
[6]Emma Guttman-Yassky, et al, Rocatinlimab: A Novel T-Cell Rebalancing Therapy Targeting the OX40 Receptor in Atopic Dermatitis. Dermatology and Therapy, 2025,Sep,(15),3153-3171


上海派思维新生物医药科技有限公司
办公地址:上海市浦东新区华夏东路333号临丰科创园5幢
人力资源 邮箱:HR@novopathway.com 电话:021-5838 0356
BD商务 邮箱:BD@novopathway.com 电话:021-5838 0618-501




