- 关于我们
- 一站式服务
- 技术平台
临床研究
临床中心实验室
临床样本病理学检测
蛋白水平检测分析
免疫学细胞表现分型分析
药物毒性检测-CRS
TMB / 免疫微环境检测
血液疾病分型检测,类型鉴定
MRD(Minimal Residual Disease)
CART/TCRT/ADC/mAb/BisAb/
临床前研究
肿瘤疾病研究平台
小分子耐药模型
原位及转移模型
肿瘤模型 | 人源化小鼠
炎症&自身免疫疾病研究平台
脓毒症、多发性硬化症模型
炎症性肠病模型
系统性红斑狼疮、肾病模型
腹泻模型精神与神经系统:疾病研究平台
阿尔茨海默症、帕金森庄模型
疼瘾、抑郁证模型
精神分裂症、脑卒中、高血压模型
代谢疾病研究平台
肝纤维化、酒精性肝炎模型
非酒精性脂肪性肝炎(NASH)模型
急性肝损伤、肥胖模型
关节和骨疾病研究平台
关节炎、痛风,性关节炎、骨质疏松症模型
类冈湿关节炎模型
呼吸系统疾病研究平台
慢性组塞性肺病(COPD)模型
急性肺损伤模型
哮喘、肺纤维化模型
肺炎链球菌、肺支原体感染模型
肺铜绿盛染、肺曲霉感染模型
心血管系统疾病研究平台
高血压、高血脂模型
衰老、动脉粥样通化、缺血性脑损伤模型
皮肤系统疾病研究平台
银屑病、系统性硬化症模型
雄秃、斑秃模型
特应性皮炎、痤疮模型
医疗器械评价研究平台
全身毒性试验/急性、亚急性、亚慢性和慢性毒性试验
生物相容性评估
医美产品医疗器械有效性,安全性评估
药代动力学、安评
体内DMPK研究、体内DMPK研究
急毒,长毒,一般毒理
安全毒理、免疫原性评价
免疫毒性评价、非GLP毒理
- 加入我们
- 联系我们
one stop service
CAR-T细胞治疗
嵌合抗原受体(CAR)-T细胞是经过基因工程改造以产生用于免疫治疗的人为干预T细胞受体的T细胞。CAR-T细胞是经精心设计,可为T细胞提供靶向特定抗原新能力的受体蛋白。要如需查看我们的CAR-T治疗工作流程,请单击此处。
CAR-T细胞治疗的流程
1. 获取患者T细胞
2. 体外制备特殊CAR-T细胞,包括T-细胞的活化,CAR-T细胞的扩增和质控。
3.治疗流程
治疗前的化疗,CAR-T细胞回输和患者临床并发症监测
4. 后续的治疗
_9w13.png)
体外试验
免疫细胞的活化与质控
用流式细胞术检测转染和活化的CAR-T细胞
.png)
(A)流式细胞术。刺激24 h后使用流式细胞仪检测CAR-T细胞群的表型和亚群组成。(B) CCK8检测。CAR-T细胞在应对EGFR抗原重复刺激的应激反应中产生增殖。(C)细胞计数法。用功能化磁珠+细胞计数法计量检测CD3阳性/CD8阴性的活性化CAR-T细胞的增殖。* p < 0.05。
CAR-T细胞的基因工程
.png)
(a)使用CRISPR/ cas9将CAR基因定点整合到TRAC基因位点。上图代表TRAC基因位点,中图代表rAAV6载体的序列中间加载CAR基因座,两侧有同源臂; 下图代表编辑过的TRAC基因位点。(b) TRAC定点整合CAR后第4天TCR/CAR流式图。(c, d) CAR+阳性T细胞的平均荧光强度(MFI) 和CAR MFI方差系数 (n=12个独立实验,6个供体)。(e)小鼠生存曲线分析。(f-j)携带NALM-6细胞系的小鼠注输1×105 CAR-T细胞(n=7 /组;每个点代表一只老鼠),并在注射后第10天和第17天将小鼠安乐死取骨髓进行CAR- T细胞和NALM-6的流式分析和计数(如e图所示)。(f) CAR-T细胞。(g)肿瘤(GFP+CD19+)细胞。(h) CAR-T细胞与肿瘤的比例。(i) CAR-T细胞第17天记忆表型(CD62L−CD45RA−)和效应表型(CD62L−CD45RA+)的百分比。(j)表达衰竭标记的CAR-T细胞百分比;第17天用流式细胞术进行量化。 * P < 0.05, * *P < 0.01, * * * P < 0.001, * * * * P < 0.0001。
CAR-T细胞的细胞因子产生和细胞毒性
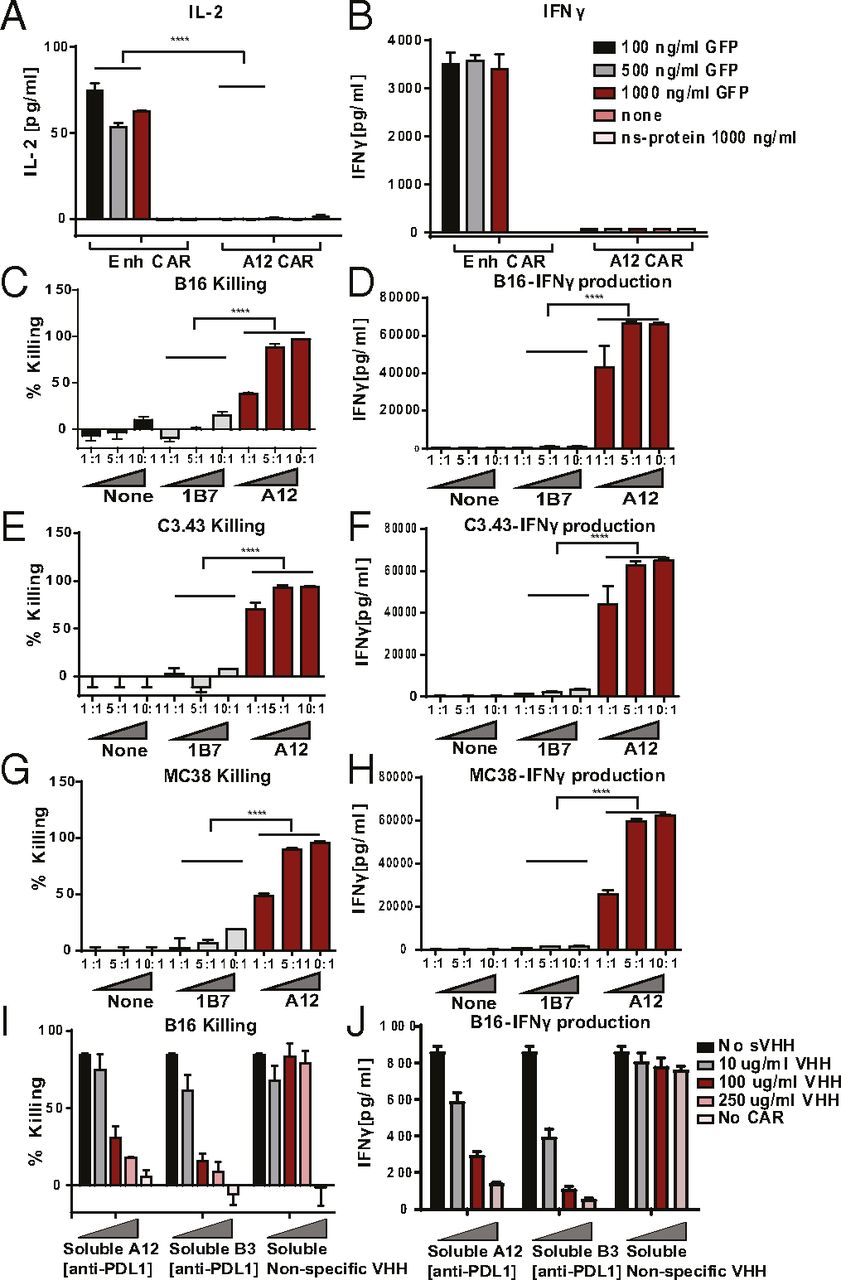
靶向EIIIB纤维连蛋白的CAR-T细胞在体内减缓B16黑色素瘤的生长。(A)用靶向EIIIB的特异性B2 CAR来转导T细胞,通过mCherry表达来测量转导效率。用重组EIIIB-GST孵育细胞,用兔抗gst和兔抗A647探针检测配受体结合。(B) B2 CAR - T细胞在对配体有识别的反应的细胞中表现出细胞毒性。B2 CAR-T细胞与表达EIIIB纤维连接蛋白结构域(AEC FN+/+)或缺乏EIIIB纤维连接蛋白结构域(AEC FN−/−)的主动脉内皮细胞(AEC)共培养。(C)小鼠在第0天接种B16肿瘤,在第4天、第15天和第20天接种B2 CAR-T细胞(n = 10)。(D)测量单个小鼠的肿瘤面积。生存曲线显示各组存活率(P = 0.0001)接受B2 CAR - T细胞治疗的小鼠存活率提高。扫描电镜如图所示。(E) RAG−/−小鼠接种B16肿瘤,并在第4天用B2 (n = 4)或1B7 CAR - T细胞(n = 3)治疗。使用B2 CAR-T细胞治疗的RAG−/−小鼠没有表现出生存改善或延缓肿瘤生长。扫描电镜如图所示。(F) MC38表达较低水平的EIIIB。
体内CAR-T药效实验
.png)
(A) NSG小鼠皮下接种2 ×10^6 NALM6细胞。接种14d后,小鼠随机分为3组,静脉注入30 × 10^6个CAR-T细胞。(B) 计量经T1或T9 CAR-T细胞治疗后小鼠的肿瘤体积。(C) CAR-T细胞治疗小鼠(n = 5) 的生存曲线图。T1与T9 CAR-T细胞治疗小鼠准确的P值通过log-rank分析显示。(D)在CAR-T回输后的指定天数内,显示治疗小鼠外周血中CAR-T细胞占比的代表性散点图。(E) CAR-T细胞输注后第8天和第12天,治疗小鼠外周血中CAR-T细胞的百分比(n = 5只小鼠)。(F) CAR-T细胞输注后第12天肿瘤浸润CAR-T细胞频率的代表性散点图(G) CAR-T细胞输注后第12天肿瘤浸润CAR-T细胞的百分比(n = 5只小鼠)。(H) NSG小鼠皮下接种3 × 106 HepG2细胞。14d后,小鼠随机分为3组,静脉注入10 ×106个CAR-T细胞。(I)接受了24天T细胞或PBS治疗的小鼠的代表性肿瘤图像。(J)用所示的T细胞或PBS处理的HepG2异种移植小鼠的生长曲线(n = 5只小鼠)。380/5000
(K)流式图(左图)和(L)汇总数据(右图);n = 4只小鼠)显示CAR-T输注后指定天数内,接受治疗小鼠外周血中CAR-T细胞的频率。(M, N) CAR-T细胞输注后第12天肿瘤浸润CAR-T细胞百分比(N = 5只小鼠)。数据以平均值±标准差表示。* * * * P < 0.05和P < 0.001。
参考文献
1. Li, H., Huang, Y., Jiang, DQ. et al. Antitumor activity of EGFR-specific CAR T cells against non-small-cell lung cancer cells in vitro and in mice. Cell Death Dis 9, 177 (2018). https://doi.org/10.1038/s41419-017-0238-6
2. Eyquem, Justin; Mansilla-Soto, Jorge; Giavridis, Theodoros; van der Stegen, Sjoukje J. C.; Hamieh, Mohamad; Cunanan, Kristen M.; Odak, Ashlesha; Gönen, Mithat; Sadelain, Michel (2017). Targeting a CAR to the TRAC locus with CRISPR/Cas9 enhances tumour rejection. Nature, 543(7643), 113–117. doi:10.1038/nature21405
3. Xie, Yushu Joy et al. “Nanobody-based CAR T cells that target the tumor microenvironment inhibit the growth of solid tumors in immunocompetent mice.” Proceedings of the National Academy of Sciences of the United States of America vol. 116,16 (2019): 7624-7631. doi:10.1073/pnas.1817147116
4. Liu, L., Bi, E., Ma, X. et al. Enhanced CAR-T activity against established tumors by polarizing human T cells to secrete interleukin-9. Nat Commun 11, 5902 (2020). https://doi.org/10.1038/s41467-020-19672-2
上海派思维新生物医药科技有限公司
办公地址:上海市浦东新区华夏东路333号临丰科创园5幢
人力资源 邮箱:HR@novopathway.com 电话:021-5838 0356
BD商务 邮箱:BD@novopathway.com 电话:021-5838 0618-501








